
Das Atommodell
Ein Atommodell (AM) ist ein Atom, die kleinste Einheit, aus der ein chemisches Element besteht. Je nachdem, ob es eine positive, negative oder neutrale Ladung hat, gibt es: Protonen, Elektronen oder Neutronen.
Das Atommodell entstand im Laufe der Jahre durch historische Ereignisse und durch die Erkenntnisse der verschiedenen Wissenschaftler, die wir Ihnen später vorstellen werden. Dieses Modell ist die Darstellung, mit der wir die Struktur des Atoms sehen können, was uns erlaubt, das Verhalten und die Eigenschaften eines Elements zu kennen.
Ziel dieser Modelle ist es, das Studium eines Materials zu erleichtern, indem die Atomtheorie in eine leichter verständliche, grafische Darstellung gebracht wird.
Wie viele atomare Modelle gibt es?
Chronologisch gesehen gibt es fünf atomare Modelle, die im Laufe der Zeit aktualisiert wurden:
- M.A de Dalton (1808)
Das Atommodell von Dalton ist das erste Modell gewesen. Dalton sagte, dass Atome nicht in kleinere Teilchen zerlegt werden können und Moleküle sich aus mehreren Bänden zusammensetzen. Außerdem werden bei einer chemischen Reaktion die Atome des Elements neu angeordnet. Dalton stellte auch fest, dass alle Atome, die zu einem Element gehören, gleich sind.

- M.A de Thomson (1904)
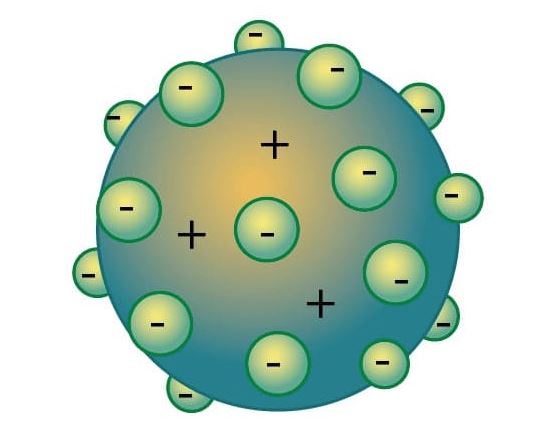
Das Thomsonsche Atommodell ging davon aus, dass Atome neutral sind. Thomson stellte fest, dass Atome passive Ladungen in Form von Protonen haben, die von Elektronen (negativen Ladungen) umgeben sind.
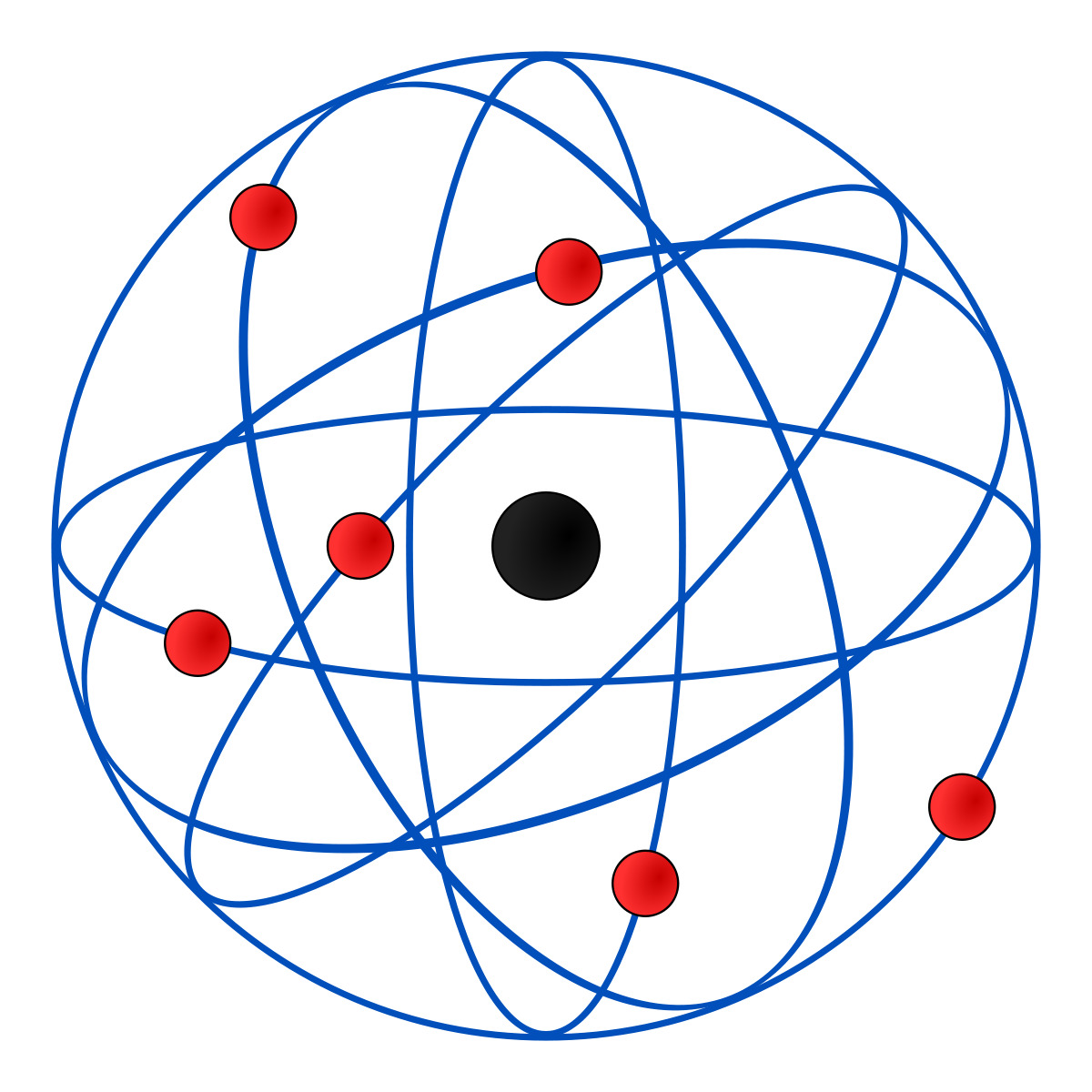
- M.A de Rutherford (1911)
Rutherford erklärte, dass ein Atom einen Kern hat, der aus positiven Ladungen besteht, die von negativen Teilchen um den Kern herum umgeben sind. Nach Rutherford waren die Atome innen leer.
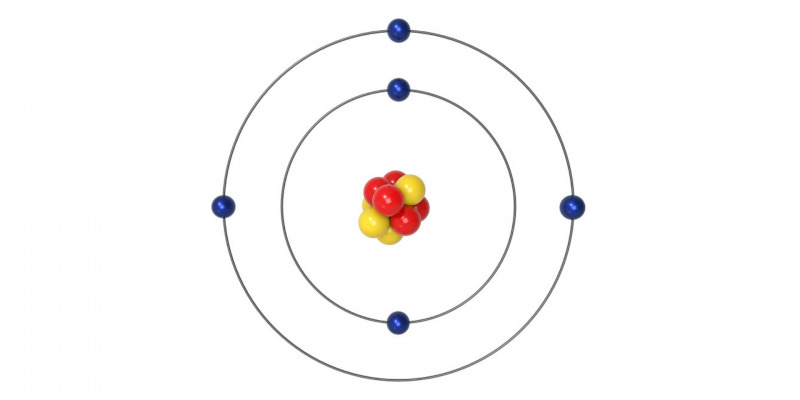
- M.A de Bohr (1913)
Niels Bohr stellte das Atom als Abbild des Sonnensystems dar, wobei die Elektronen die Planeten und der positiv geladene Kern die Sonne darstellten.
- M.A de Schrödinger (1926)
Dieses Modell erklärt das Gleichgewicht, das zwischen Molekülen und chemischen Bindungen besteht. Hier finden wir Elektronen mit unterschiedlichen Energieniveaus, je nach dem Vorhandensein des magnetischen und elektrischen Feldes.

Das heutige Atommodell wurde 1920 von Schödinger und Heisenberg entwickelt. Das derzeitige Atommodell ist ein mathematisches Modell, bei dem sich die Elektronen in Energieniveaus befinden und eine wellenförmige Bewegung ausführen.